Thèse de Doctorat d'état es sciences physiques
présentée à l’Université Paris VI
pour obtenir le grade de Docteur-es Sciences
par
Jean-Christophe Doré
Nouveaux antitumoraux de
synthèse au départ de l'acide aristolochique. Mise en évidence d'un groupement
actif dans leur molécule et proposition d'un mécanisme probable de leur mode
d'action chimique au niveau cellulaire
soutenue le 22 avril 1974
devant la commission d'examen :
Rigaudy, J., président
Basselier, J. J., Poisson, J., Rumpf, P., et Viel,
C., examinateurs
«La
clef de toutes les sciences est sans contredit le Point d'Interrogation ; nous devons la plupart des grandes
découvertes au Comment ?
et la sagesse dans la vie consiste peut-être à se demander, à tout propos, Pourquoi ?"
H.
de BALZAC
(La peau de chagrin, II)
cependant
«L'ignorance qui estoit naturellement en nous, nous l’avons
par longue estude confirmée et avérée".
MONTAIGNE
(Essai, Livre II, Ch. XII)
INTRODUCTION
Les Aristolochiacées comprennent des plantes vivaces herbacées ainsi
que des lianes à feuilles alternées simples et à fleurs solitaires ou
disposées en grappes ; leur répartition géographique, très étendue, couvre
tous lescontinents. Le nombre des
espèces est important puisque PFLUGE en a recensé 36 distinctes.
L'intérêt attaché à ce type de plantes est fort ancien puisqu'on
les utilisait en thérapeutique dès l'époque gréco-romaine. C'est ainsi que
LEMERY à la fin du 17ème siècle procède à une étude pharmacognosique
détaillée de cette famille botanique, dans son traité de chimie et dans son
Dictionnaire Universel des Drogues. De nos jours encore, les sorciers
Africains utilisent des extraits de ces plantes en médecine tribale, selon
des recettes ancestrales.
Cet aspect thérapeutique avait
suscité des recherches sur la nature et la composition des différents
principes actifs rencontrés dans ces plantes. De nombreux travaux répertoriés
dans une mise au point récente ont permis de mettre en évidence qu'en dehors
des terpènes; des flavones, des aporphines et de divers composés classiques
dans les extraits végétaux, on rencontre essentiellement des substances
nitrophénanthréniques dont la structure particulière est caractéristique de
cette famille botanique. L'originalité et la complexité relative de ces
molécules a longtemps retardé la détermination exacte de leur structure : ce
sont les travaux de PAILER et de ses collaborateurs qui ont permis
d'attribuer la structure 1 (méthylènedioxy-3,4 méthoxy-8 nitro-10
phénanthrène carboxylique-1) à l'acide aristolochique ou acide aristolochique
I, produit principal caractéristique de toutes les espèces d'Aristoloches
étudiées. Cette structure a été définitivement confirmée quelques années plus
tard, après que KUPCHAN et ses collaborateurs aient, en 1965, décrit une
synthèse totale de cet acide.
Les produits que nous avons synthétisés et testés sont numérotés
en chiffres arabes, alors que des chiffres romains -ont été adoptés pour tous
les autres composés cités dans le texte.
A ce jour, un certain nombre
de molécules naturelles dérivés de cette structure ont été isolées et
caractérisées : il convient de citer notamment un produit de dégradation,
l’aristolactame II, les acides aristolochiques III, IV et V, l'acide débilique
VI et le "rouge aristo" (aristo red) VII.
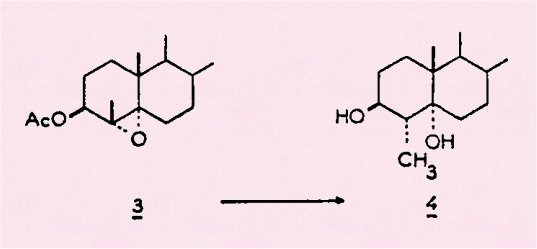
La présence de ce type de structures inhabituelles comme
produits du métabolisme végétal tend à s'expliquer par une oxydation de
structures aperphiniques dont la mise en évidence a été effectuée dans
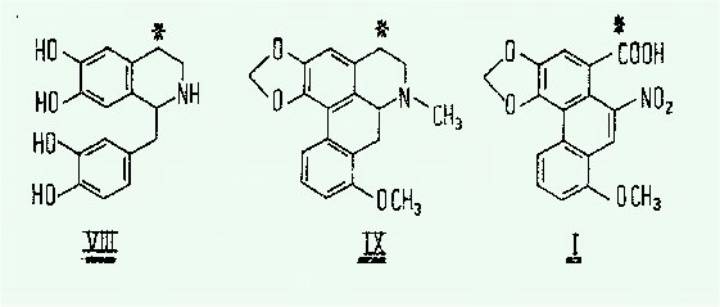
certaines espèces d’Aristoloches (9, 10) : c'est ainsi que la stéphanine
IX, présente dans ces plantes, parait être un précurseur direct de l'acide
aristolochique. En effet, d'études réalisées sur Aristolochia siphe l’Her.,
il ressort que l'administration de chlorhydrate de nor-landanesine 4-C14 VIII
conduit à 1’acide aristolochique marqué sur son carboxyle, et que celui-ci ne
peut se former que par l’intermédiaire de la stéphanine
La littérature fait très largement mention des propriétés
thérapeutiques des extraits des différentes aristoloches qui ont été
largement utilisées et le sont encore en médecine indigène (12) pour
faciliter les accouchements, comme antidotes contre les effets des morsures
de serpents, comme toniques, fébrifuges, antispasmodiques et purgatifs.
D’autre part. des travaux récents ont montré que les extraits d'Aristololochia
clématis L. présentent des propriétés antibactériennes remarquables, inhibant
fortement les cultures de Staphylococcus aureus, et que les extraits
d'Aristolochia elegans Hast. présentent une activité antimitotique (15)
vis-à-vis des cellules de graines d’oignon en germination.
La séparation et la purification du principe actif essentiel,
l’acide aristolochique, a permis aux pharmacologues de reprendre l'examen des
différents aspects des propriétés thérapeutiques attribuées à cette famille
botanique et de vérifier que l'acide aristolochique est bien responsable des
propriétés observées parmi lesquelles les propriétés antibactériennes et
antitumorales sont les plus intéressantes.
L’action bactériostatique a été vérifiée in vivo par inhibition
du pneumocoque, l’acide aristolochique prolongent de façon sensible le temps
de survie de souris infectées par cet agent microbien. D'autres travaux
présentent des conclusions moins catégoriques concernant l'effet de cet acide
vis-à-vis d'autres espèces bactériennes. En revanche la stimulation de la
phagocytose par l’acide aristolochique est remarquable : après infection
par Mycobactérium tuberculosis le pourcentage de cobayes survivant est bien
supérieur pour les animaux traités par l'acide aristolochique. Cet acide
stimule de façon sélective la phagocytose de nombreuses espèces microbiennes
par les leucocytes sanguins, tant dans des expériences faites sur les
animaux, que dans celles qui sont pratiquées avec le sérum humain.
L’inhibition tumorale est
la seconde propriété pharmacologique intéressante. Ainsi, après les travaux
de BARNARD, déjà cités il se confirme
que les extraits d’Aristolochia indica L., comme ceux d'Aristolochia elegans
mast inhibent les tumeurs expérimentales chez l'animal et que seul l'acide
aristolochique est responsable de cette activité qui se manifeste sur
1 adénocarcinome ÇA 755 de la souris en particulier. Par ailleurs, cet acide
provoque l'arrêt de la croissance des cellules tumorales humaines.
FILITIS et MASSAGETOV ont
montré également que des injections intrapéritonéales répétées d'acide
aristolochique inhibent la croissance de l'heptoma ascitique du rat, mais
n'ont, en revanche, aucun effet sur le développement de sarcome 45 et M1 et
le carcinome RS1 du rat. Les recherches en chimiothérapie antitumorale au
départ de l'acide aristolochique ont été quelque peu freinées par suite de
cette absence d'activité surtout de souches tumorales et par le fait que,
lors d'essais cliniques, JACKSON ait montré que la toxicité rénale limite l'éventuel
emploi de cet acide en thérapeutique humaine en deçà des doses curatives.
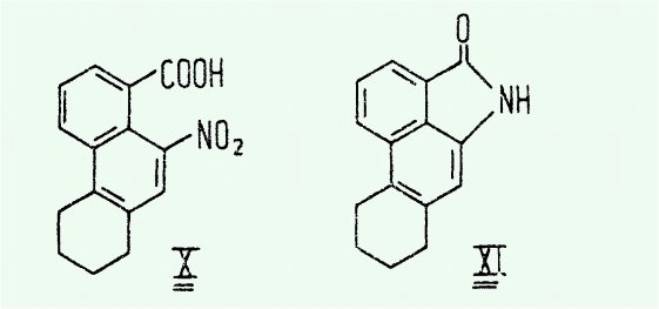
A notre connaissance, seuls
KUPCHAN, WORMSER et MOKOTOFF ont entrepris la synthèse de plusieurs composés
phénanthréniques analogues à l'acide aristolochique. Parmi ceux qui ont été
testés, l'acide nitro-10 tétrahydro-5,6,7,8 phénanthrène-carboxylique-1 X et
son lactame XI n'exercent aucune action inhibitrice vis-à-vis des cellules
tumorales en culture ; il en est de même pour le lactame II de l'acide
aristolochique.
En ce qui concerne
les études toxicologiques postérieures à celles de JACKSON, une analyse
sommaire ferait apparaître des contradictions entre les conclusions des
différents travaux. En effet, si CONCHA et ses collaborateurs confirment la
toxicité rénale et hépatique de l'acide aristolochique dans des essais
systématiques réalisés chez différents animaux, corroborant ainsi les
résultats de l'étude clinique de JACKSON, en procédant à l'étude clinique de
cet acide comme excitant de la phagocytose, SCHULZ, WEISS et GEMAHLICH
signalent qu'aucun effet toxique n'a été observé chez l'homme. Ces
divergences s'expliquent si l'on considère que ces deux types de propriétés,
antitumorales et prophagocytaires se manifestent à des doses thérapeutiques
très différentes, autour de 1mg/Kg chez la Souris pour les premières et vers
0,02 mg/Kg pour les secondes. Or si la DL.50 se situe à 16 mg/Kg chez la
Souris, le seuil de toxicité chronique est beaucoup plus bas, de l'ordre de 1
à 2 mg/Kg chez ce même animal, ce qui confirme les premières constatations de
JACKSON.
Les considérations qui
précèdent, ainsi que le très petit nombre des travaux concernant les
modifications de la structure de bas de l'acide aristolochique, nous ont
incité à nous engager dans cette voie de recherche, D’autant plus que la
présence d'un noyau phénanthrénique est assez peu répandue dans les
structures de produits issus du métabolisme végétal et que les produits
naturels nitrés sont très rares. Toutes ces caractéristiques chimiques
confèrent à la structure de l'acide aristolochique une originalité certaine
par rapport aux familles d'alcaloïdes classiques. D'autre part, la relative
complexité de la molécule pouvait laisser supposer que des analogues
simplifiés seraient peut-être moins toxiques et présenteraient une activité
comparable ou même supérieure à celle de la molécule modèle dont on a vu que
la toxicité limite l'utilisation thérapeutique, d'une manière rédhibitoire
Les indications de la
littérature relatives à l'activité antitumorale des molécules qui possèdent
une des trois fonctions caractéristiques de l'acide aristolochique, sont peu
significatives. En ce qui concerne la partie phénanthrénique, des centaines
de substances à noyaux aromatiques condensés ont été testées, mais pour les
molécules douées d'un haut niveau d'activité le ou les groupements greffés
sur le squelette phénanthrénique peuvent être considérés, de toute évidence,
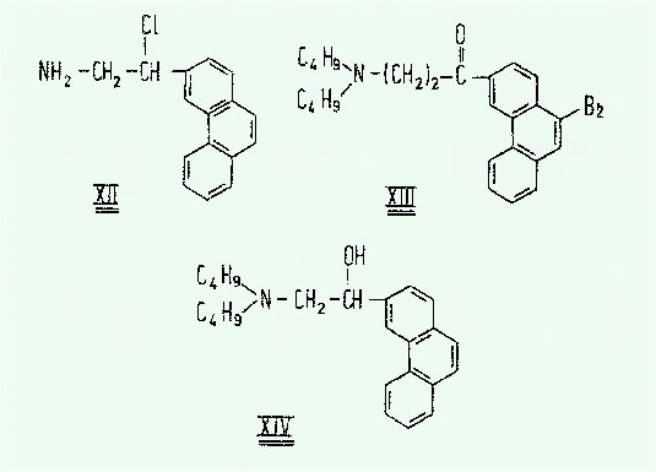
comme les principaux responsables des effets observés. Il en est ainsi pour
les composés des types XII, XIII, XIV, dont une mise au point récente signale
l'excellente activité.
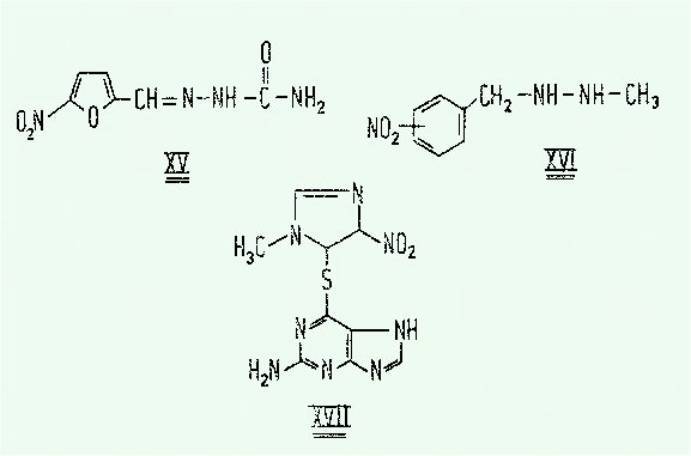
Parmi les molécules nitrées
douées d’un pouvoir antitumoral, on peut relever la nitrofurasone XV, la
myélone XVI et la thiamiprime XVII.
Aucune corrélation simple
n'apparaît entre les structures de ces composés et cette activité.
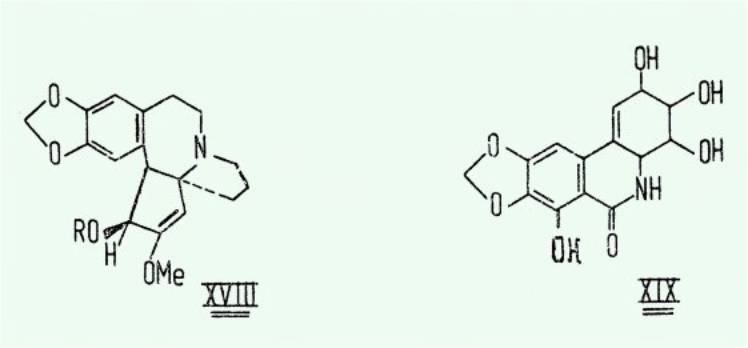
Quant au groupement
éthylènedioxyle, on note sa présence dans des molécules naturelles possédant
une activité antitumorale, telles que l'hanmgtonime XVIII, la narciclasine
XIX, la podophyllotoxine XX, et le burseran XXI par exemple.
On ne voit, ici encore,
aucune corrélation permettant d'orienter les recherches vers un motif plus
simple, doué des mêmes propriétés.
Cette première tentative
d'approche montre que, sans négliger une démarche analytique basée sur
l’étude des propriétés biologiques de molécules possédant une des fonctions
de l'acide aristolochique prise isolément ou simultanément deux d'entre
elles, il est, de toute évidence, nécessaire d'envisager un cheminement plus
rationnel portant sur des modifications limitées du nombre, de la nature et
de la position des substituants, à partir de l'acide aristolochique pris dans
sa pluralité fonctionnelle. Une voie intermédiaire peut aussi être
envisagée : elle consiste à modifier le squelette phénanthrénique, tout
en respectant la nature des fonctions de la molécule modèle.
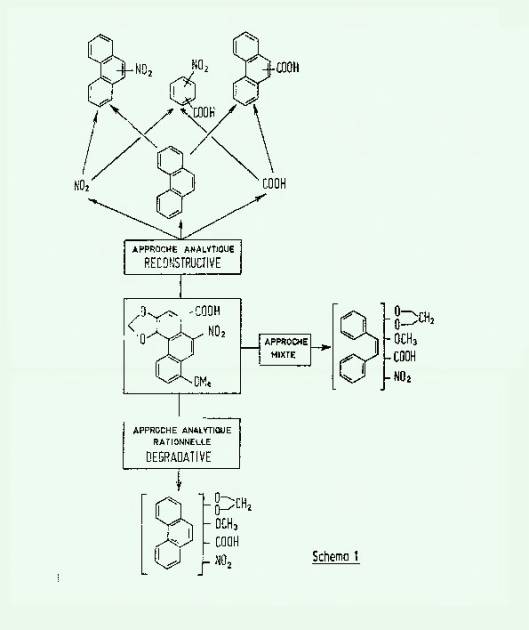
Ces différentes démarches
expérimentales sont résumées dans le schéma I et seront développées dans les
chapitres suivants de ce travail. On verra que nos recherches dans le domaine
des analogues simplifiés de l'acide aristolochique se sont révélées
fructueuses, un grand nombre de séries étudiées s'étant avérées cytotoxiques
sur cellules tumorales en culture, et cette activité nous a conduit à
envisager une hypothèse concernant leur mode d'action chimique, au niveau
cellulaire, hypothèse que nous avons vérifiée par ailleurs en procédant à des
études cinétiques simples et à une analyse prévisionnelle de la structure
active optimale, par des calculs de mécanique ondulatoire. Ce sont ces
résultats qui font l'objet de notre mémoire.
CONCLUSION
Arrivé au terme de cet
exposé, il importe d’établir un bilan des résultats obtenus, et d'examiner
les perspectives de recherches offertes par ce travail.
Nos résultats ont montré,
sur le plan pharmacologique qu’un nombre considérable de composés possédant
le groupement nitrovinylique de l'acide aristolochique sont doués d'activité
cytotoxique antitumorale, mais que, si ces propriétés se vérifient in-vivo
sur ascite de KREBS, il n'est pas de même sur la souche L.1210.
Cependant, il ressort
de notre étude qu’une possibilité d'utilisation de ces composés en
thérapeutique humaine est improbable, par suite d'une variation parallèle de
leur activité antitumorale et de leur toxicité, ce qui revient à dire que
leur coefficient chimiothérapeutique est toujours faible. Toutefois, on peut
envisager d'écarter cette difficulté en associant deux notions déjà évoquées
au cours de travail : celle de site actif masqué et celle de groupement
vecteur. Des composés a double liaison éthylénique activée potentielle sur
lesquels seraient greffes des radicaux susceptibles de constituer des
maillons élémentaires de synthèse cellulaire et d'assurer leur transfert à
travers un organisme vivant, pour-raient peut-être apporter une réponse au
problème posé.
L'apport principal de notre
travail parait donc se situer exclusivement sur le plan de la recherche
fondamentale : établissement d'une corrélation entre l'activité antitumorale
de diverses séries de molécules et leur possibilité de se fixer sur des sites
nucléophiles cellulaires. En ce qui concerne leur
place dans la classification des produits antitumoraux, les composés que nous
avons préparés et étudiés constituent une nouvelle classe de molécules
actives qui peuvent être rangées parmi les agents alcoylants, mais sont
spécifiquement caractérisés par la présence d'une double liaison éthylénique
activée constituant le support reconnu de leur activité.
On peut situer dans cette
nouvelle classe, des composés électrophiles dont les actions antitumorales
avaient été signalées antérieurement et qui renferment dans leurs molécules
une double liaison activée : méthylènes-lactones macrocycliques,
sarcomycine, aldéhyde triméthoxy 3,4.5 cinnamique. Leurs effets antitumoraux
résultent vraisemblablement du même mode d'action chimique au niveau
cellulaire.
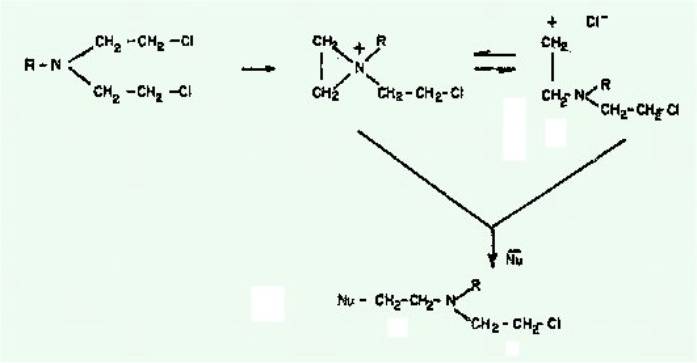
D'autre part, le
parallélisme avec les agents alcoylants classiques (moutardes à l'azote,
éthylène-imines, époxydes. etc.) réside à la fois dans l'absence de
sélectivité de l'action thérapeutique et dans la similitude de l'action
chimique. Il est, en effet, démontré que l'activité antitumorale des
moutardes à l'azote et des éthylène-imines est liée à l'addition d'un groupe
nucléophile, au niveau cellulaire, selon le schéma :
Par ailleurs, si l'on
considère que le groupement nitrovinyle plus ou moins conjugué est à
l'origine de l'activité biologique, on peut penser qu'un groupe nitro en
position mésophénanthrénique serait susceptible de conduire dans certains
cas. à des molécules antitumorales. Il parait donc intéressant d'envisager la
synthèse de produits doués d'une telle activité à partir d'hydrocarbures
cancérogènes ni très sur leur zone K, On a signalé, en effet, que le pouvoir
cancérogène de ces hydrocarbures disparaît après nitration en zone méso (cas
du benzo-3,4 pyrène).
Des recherches dans ce sens
permettraient peut-être d'éclaircir un domaine assez controversé de la
chimiothérapie antitumorale, celui qui concerne la coexistence de propriétés
antagonistes dans une même famille chimique. On peut envisager deux types
d'addition distincts avec les électrons II d'une double liaison
pseudo-éthylénique provoquant soit une induction soit une inhibition de la
cancérogenèse : de nombreux auteurs interprètent, en effet. l’activité
tumorigène des hydrocarbures aromatiques à cycles condensés par une
interaction de leur zone K et, accessoirement, de leur zone L, avec des
protéines cellulaires, et par ailleurs, nos résultats indiquent que
l’addition d'un groupement nucléophile selon MICHAEL exerce un effet
contraire. En résumé, par toutes les
questions qu'elles soulèvent ces recherches paraissent devoir être le point
de départ de nouveaux travaux en chimie antitumorale.