Thèse
présentée à Faculté des sciences de l'Université de Lyon
pour
obtenir le grade de Ingénieur-Docteur
par
pour obtenir le grade de Ingénieur-Docteur
par
Alain Guyot
Contribution à l'étude des chromanones-4
soutenue
le 12 janvier1957
devant
la commission d'examen :
Prettre,
M., président
Colonge, J., Mentzer, C.,
examinateurs
INTRODUCTION
On appelle Chromanones ou
Dihydrobenzopyrones des composés possédant, accolé à un noyau benzénique, un
hétérocycle oxygéné à 6 atomes, sur lequel est fixée une fonction cétone ;
selon la place de cette dernière, on distingue trois classes de chromanones :
Chromanones-2, -5 ou -4
La numérotation de
tels systèmes est faite comme l’indique le schéma ci-dessous :
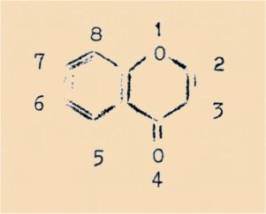
Nous nous sommes intéressés
seulement aux chromanones-4. Bien qu’une somme de travaux non négligeable ait
été consacrée à ce sujet, l’étude des chromanones-4 est loin de pouvoir être
considérée comme complète.
Il nous a paru intéressant de
rechercher une méthode de préparation simple et efficace, à partir de matériaux
facilement accessibles. De plus, nous avons tenté de mettre en lumière quelques
propriétés nouvelles ou peu connues de ces corps.
Notre travail comportera donc deux
parties principales:
- Ière Partie : Préparation de
Chromanones-4
- IIème Partie : Etude de
propriétés des Chromanones-4
CONCLUSIONS GENERALES
Nous pouvons dégager de cette étude
les conclusions ci-après :
1) L’étude de la cyanoéthylation de douze phénols nous a pemis
d'établir ou de vérifier les points suivants :
a. la réaction est limitée et
réversible en milieu alcalin
b. le rendement dépend de la nature et de la position des substituants
; en particulier, la présence d'un radical en ortho de la fonction alcool
abaisse considérablement le rendement.
c. dans le cas des diphénols, les deux fonctions alcool réagissent et
il n'est pas possible d'obtenir des produits mono-cyanoéthylés.
d. la présence d'un substituant sur l'un des atomes de carbone de
l'acrylonitrile abaisse considérablement le rendement de la réaction, otant
ainsi tout intérêt pratique à cette opération.
2) Les b-aryloxypropionitriles obtenus sont très sensibles à l'action
des agents alcalins qui provoquent la rupture du pont étheroxyde et
reconduisent aux phénols. Le passage de la fonction nitrile à la fonction acide
ne peut donc se faire dans ce cas que par hydrolyse en milieu acide; les
rendements sont alors très satisfaisants.
3) Dans la réaction de cyclo déshydratation des acides b-aryloxypropioniques en chromanones-4, la substitution du mélange
acide-anhydride phosphoriques en proportions convenables à l'anhydride
phosphorique seul permet, outre une économie de réactif, d’élever notablement
le rendement qui peut alors atteindre 80% dans les cas les plus simples.
4) La condensation de l’acide b-chloroisobutyrique
sur les phénols est moins facile que celle de l'acide b-chloropropionique. Elle ne peut se faire que sur des phénols
simples, et l'emploi obligatoire d'un milieu réactionnel alcalin limite les
rendements .à des valeurs faibles
5) La fonction cétone des chromanones-4 réagit normalement. On obtient
facilement les oximes et semicarbazones. La condensation sur les glycols
conduit à des produits peu stables. Enfin la réaction de GRIGNAKD est normale
et se fait avec des rendements excellents; les chromanols -tertiaires obtenus
se déshydratent facilement en A-3-chromènes. Ces derniers corps sont
extrêmement sensibles à l'action de l'oxygène aussi ne peut-on envisager
d'utiliser leurs propriétés réactives sans opérer en atmosphère inerte.
6) Le carbone 5 de l'hétérocycle, en a de la fonction cétone, est très
reactif et on peut substituer de nombreux radicaux aux atomes d'hydrogène qu'il
porte. Toutefois les chromanones sodées sont très instables, et le
tertioamylate de sodium est le seul agent qui nous a permis d'obtenir des
méthyl-3 chromanones-4, par l'action de l'iodure de méthyle sur les chromanones
ainsi sodées.
La substitution du brome aux atomes
d'hydrogène du carbone-3 est extrêmement aisée et permet d'obtenir de nombreux
dérivés: bromo et dibromochromanones, amino chromanones, chromones
bromochromones, et aminochromones.
Nous avons fait une étude spectrographique
infrarouge de la chromanone-4 et de quelques dérivés. Malgré l'absence dans la
littérature de spectres de produits analogues, on peut vérifier quelques points
de la structure des composés étudiés: noyau aro-matique orthodisubstitué,
fonction cétone conjuguée, présence éventuelle d'une double liaison éthylénique
ou de groupements méthylène. En particulier, on vérifie que le produit
monobromé F = 65° de ARNDT ne possède pas de double liaison éthylénique et
qu'il n'est pas la Bromo-5 chromone.
Au cours de cette étude nous avons préparé
un certain nombre de produits nouveaux. On trouvera dans les pages suivantes
leurs principales constantes physiques.
Mots clefs :
acide / action / agent / atome / bromochromone / carbone / cétone / chloroisobutyrique /
chloropropionique / chromanol / chromanone / chromène / chromone / cyanoéthylation / diphénols /
étheroxyde / étude / fonction / hétérocycle / liaison / méthyle / noyau / oxime / phénol /
phosphorique / préparation / propriété / reactif / réaction / rendement / spectrographique /
structure / substituant / substitution