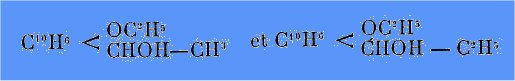Thčse présentée ą la faculté des sciences de Paris
pour obtenir le grade de Docteur és-sciences physiques
par
André HELBRONNER
CONTRIBUTION A L'ETUDE DES ALDEHYDES OXYNAPHTOIQUES
soutenue en février 1946
devant la commission d’examen :
Bouty, président
E. Ditte, Haller, examinateurs
INTRODUCTION
Ce travail a pour objet l'étude des aldéhydes oxynaphtoļques de leurs dérivés et de leurs produits de condensation.
On peut théoriquement prévoir l'existence d'un grand nombre d'aldéhydes dérivant des
naphtols a et b et répondant
indistinctement ą la formule générale :
Pratiquement les réactions donnant naissance ą ces corps ne fournissent qu'un seul aldéhyde sans mélange d'isomčre.
Dans le cas du b naphtol le groupe aldéhydique se place en position ortho par rapport ą l'hydroxyle phénolique.
Dans le cas de l'a naphtol les deux groupes prennent la position para l'un par rapport ą l’autre.
Leurs formules de constitution seront donc :
L'étude de ces corps a été entreprise dans le but principal de fixer les différences pouvant se manifester chez les aldéhydes aromatiques quand on passe du noyau benzénique au noyau naphtalique.
Nous avons envisagé tout d'abord les modes d'obtention des aldéhydes naphtoļques, mais les préparations indiquées, soit par Bamberger, soit par Rousset, sont longues et difficiles, aussi avons-nous préféré entreprendre l'étude des aldéhydes oxynaphtoļques dont l'obtention est aisée.
Ce travail sera divisé en deux parties :
Premičre partie. — Etude de l'aldéhyde boxynaphtoļque ou b oxynaphtal.
CHAPITRE I. — Préparation, Constitution, Propriétés du b
oxynaphtal.
CHAPITRE II. — Ethers.
CHAPITRE III — Condensation avec les cétones.
a) Condensation avec le camphre.
b) Condensation avec les éthers acétylacétiques.
c) Condensation avec l'acétylacétone.
d) Condensation avec l'acétophénone.
CHAPITRE IV — Condensations diverses
a) Condensation avec l'éther malonique.
b) Condensation avec l'éther cyanacétique.
c) Condensation avec la diméthylaniline.
Deuxičme partie. — Etude de l'aldéhyde a oxynaphtoļque ou a oxynaphtal.
CHAPITRE I. — Préparation, Propriétés, Constitution de a
Oxynaphtal.
CHAPITRE II. — Ethers.
CHAPITRE III. — Condensation avec le camphre.
CHAPITRE IV — Condensations diverses
a) Condensation avec la diméthylaniline.
b) Réaction de Grignard.
c) Condensation avec le b naphtol.
Enfin quelques conclusions termineront ce travail.
Premičre partie: B Oxynaphtal.
1° J'ai étudié la préparation du B Oxynaphtal par la réaction de Roemer et Tiemann ; j’ai montré qu’il était possible de l’effectuer avec de bons rendements en molieux aqueux.
2° J’ai préparé les éthers méthyliques, éthyliqnes, propyliques, du B Oxynaphtal par application de la réaction de Gattermann et par action des lodures alcooliques sur le B Oxynaphtal sodé.
J'ai étudié quelques dérivés de l’éther éthylique (picrate, Phénylhydrazone imines), j’ai obtenu également l'éther acétique et l’éther benzoļque ; enfin j’ai condensé le B Oxynaphtal avec l’iodure de méthylčne et l’iodacétate d’éthyle.
3° J’ai condensé les éthers du B Oxynaphtal avec le camphre et préparé ainsi des composés ą noyau naphtalique analogues ą ceux obtenus par M. Haller dans la série benzénique ; j’ai constaté que ces condensations s’effectuaient avec formation d’un éther de l’acide oxynaphtoļque et qu’ainsi la théorie de la réaction donnée par. M. Haller s’appliquait également dans le cas de cet aldéhyde ; j’ai opéré la réduction des corps de condensation obtenus ; j’ai montré qu'ils pouvaient fixer le brōme ; enfin, j’ai étudié leurs propriétés optiques.
4° J’ai effectué la condensation du B Oxynaphtal avec l’acétylacétate d’éthyle au moyen de l'acide chlohydrique ; j’ai obtenu ainsi un chlorhydrate dont la composition correspond ą celle du chlorhydrate que l on pourrait obtenir avec la naphtocoumarine méthylcétone préparée antérieurement.
J’ai constaté que ce dernier composé ne fixait pas l’acide chlorhydrique et montré ainsi
que la théorie de Vorländer relative ą la constitution des chlorhydrates de cétones non
saturées est inapplicable ici.
J'ai préparé le mźme chlorhydrate par fixation d'acide chlorhydrique sur l’acide coumarique de la naphtocoumarine méthylcétone.
J'ai expliqué ces différents faits en m'appuyant sur l'hypothčse de Michael relative ą la constitution des acides coumariques, j'ai été ainsi conduit ą assigner au chlorhydrate obtenu la formule suivante :
qui en fait un éther chlorhydrique et explique en outre ses propriétés colorantes.
5° J'ai effectué la condensation du B Oxynaphtal avec l’acétophénone au moyen de l'acide chlorhydrique ; j'ai obtenu ainsi le chlorhydrate du B Oxynaphtalacétophénone ; j'ai adopté pour la constitution de ce chlorhydrate l'hypothčse de Baeyer sur la tétravalence de l'oxygčne et ai par conséquent assigné ą ce corps la formule :
6° J'ai effectué la condensation de l'Ethoxynaphtal avec l'acétylacétone au moyen de l'alcoolate de sodium ; j'ai constaté que dans ces conditions il y avait rupture de la molécule d'acétylacétone et formation de :
7° J'ai effectué la condensation du B Méthoxynaphtal avec l’éther malonique en me servant d'un mélange d'anhydride acétique et de chlorure d'acétyle comme déshydratant, j'ai, ainsi obtenu :
8° J'ai effectué la condensation du B Ethoxynaphtal avec le cyanacétate d'éthyle par fusion directe des deux corps ; j'ai étudié quelques-unes des propriétés du corps de condensation obtenu :
9° J'ai étudié la couleur fournie par l'oxydation du produit de condensation du B Oxynaphtal avec la diméthylaniline.
Deuxičme partie : A Oxynaphtal.
1° Pour bien caractériser l'A Oxynaphtal obtenu par Gattermann j'ai préparé quelques-uns de ses dérivés immédiats (picrate, imines, etc.).
2° J'ai constaté que l'oxydation de l'aa Oxynaphtal — particuličrement au moyen du permanganate de potasse — fournissait de la paranaphtoquinone.
3° J'ai préparé les éthers méthylique, éthylique, propylique, acétique, benzoļque de l'aa Oxynaphtal, ainsi que quelques dérivés de l’éther éthyllque (Picrate, phénylhydrazone).
4° J'ai effectué la condensation de l'aa Ethoxynaphtal avec le camphre.
Dans la réaction donnant naissance ą :
il se produit également un acide éthoxynaphtoļque que j’ai identifié avec l'acide éthoxynaphtoļque 1.4.
L'obtention de cet acide m'a permis de fixer la constitution de l'aa Oxynaphtal qui est l'oxy aldéhyde naphtoļque.
J'ai constaté que l’aa Ethoxynaphtalcamphre a mźme pouvoir rotatoire spécifique que l'a b ethoxynaphtal-camphre.
5° J'ai constaté que l'AA Oxynaphtal ne se combine pas avec la diméthylaniline ; l'AA Ethoxynaphtal par contre se condense avec deux molécules de ce corps pour former un leuco-dérivé qui par oxydation donne une matičre colorante dérivée du diphénylnaphtylméthane.
6° J'ai appliqué la réaction de Grignard ą l'AA Ethoxynaphtal et obtenu ainsi les alcools secondaires:
7° J'ai condensé l'AA Oxynaphtal et l'AA Ethoxynaphtal avec le B Naphtol au moyen de l'acide chlorhydrique et obtenu ainsi des dérivés du trinaphtylméthane :
J'ai identifié ce dernier composé avec le corps obtenu par éthylation du premier.
MOTS CLEFS :
acide / aldéhyde / camphre / chlorhydrate / condensation / constitution / dérivé / diméthylaniline / éther / éthoxynaphtal / éthyle / formule / gattermann / grignard / haller / méthylcétone / naphtalique / naphtocoumarine / naphtol / oxynaphtal / oxynaphtoļque / phénylhydrazone / préparation / propriété / réaction